И. Г. Хомченко, А. В. Трифонов, Б. Н. Разуваев. "Современный аквариум и химия". г. Москва, "Новая волна".
КИСЛОТА ИЛИ ЩЕЛОЧЬ?
Рассказывая об электролитах, мы уже упоминали понятие «кислота» и
«щелочь». Отличительная особенность кислот — создание в растворе повышенной
концентрации ионов водорода H+ (за счет электролитической
диссоциации). Именно эти ионы придают кислый вкус растворам и обусловливают
целый ряд других свойств. Чем больше в растворе ионов водорода, тем более
кислой будет вода. Главная особенность щелочей — увеличенное по сравнению с чистой водой
содержание гидроксид-ионов ОН‾. Чем выше концентрация этих ионов, тем
более щелочным является раствор.
Можно ли количественно оценить кислотные и щелочные свойства воды и
этих растворов? Можно. Удобнее всего использовать для этого водородный
показатель, который в аквариумной литературе иногда называют показателем
активной реакции воды. Водородный показатель обозначают символом pH. Его легко
вычислить, если известна молярная концентрация ионов водорода в растворе c(H+)
(в моль/л). Тогда
|
pH = -lg c(H+), |
(7) |
т. е. водородный показатель
— это десятичный логарифм молярной концентрации ионов водорода, взятый со
знаком «минус».
Чему равен водородный показатель
в чистой воде? Его легко рассчитать, если воспользоваться рассмотренным нами
понятием «ионное произведение воды». Как было сказано, в чистой воде
концентрации ионов H+ и OH‾ равны, т. е. c(H+) =
c(ОН‾). Учитывая, что c(H+) • c(ОН‾) = 10‾ 14 (см. формулу 6), получаем:
c(H+)
• c(ОН‾) = (10‾ 14)1/2 =10‾ 7
моль/л.
Теперь можно рассчитать
водородный показатель
pH = - lg c(H+); pH = - lg 10‾ 7 = 7.
Таким образом, в чистой воде
значение водородного показателя равно 7. Водная среда с таким значением pH
называется нейтральной.
Теперь предположим, что в
воду добавили кислоту, например, соляную HCl.
Кислота диссоциирует на ионы:
HCl = H+ + Cl‾
Из уравнения следует, что в
растворе увеличивается концентрация ионов H +, причем тем сильнее,
чем больше мы добавим кислоты. Следует отметить, что концентрация ионов
ОН‾ при этом уменьшается за счет образования воды из ионов:
OH‾ + H+ = H2O
Как изменится pH при этом?
Очевидно (см. формулу 7), что pH будет уменьшаться, причем он будет тем меньше,
чем больше концентрация кислоты. Таким образом, в кислой среде значение pH
меньше 7.
Если в воде растворить
щелочь, например, NaOH, то в результате процесса диссоциации
NaOH = Na+ + ОН‾
в растворе увеличится
концентрация ионов ОН‾. Учитывая, что произведение c(H+) • c(OH‾) должно оставаться постоянным (ионное
произведение воды), делаем вывод: концентрация ионов H+ падает, а pH
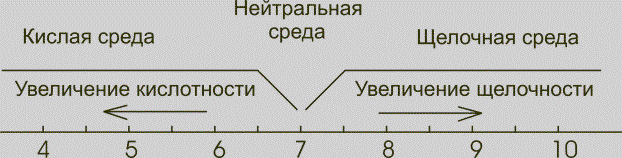
растет, т. е. становится больше 7. На рис. 3 показана шкала pH в водных
растворах.
Рис. 3.
Шкала pH в водных растворах
В аквариумной литературе
различные интервалы pH получили следующие названия: pH < 3 — сильно — кислая
вода; pH 3—5 — кислая; pH 5—б — слабокислая; pH 6—7 — очень слабокислая; pH 7 —
нейтральная; pH 7—8 — очень слабощелочная; pH 8—9 — слабощелочная; pH 9—10
щелочная и pH > 10 — сильнощелочная.
Пример. Водородный показатель воды в
двадцатилитровом аквариуме равен 7. Рассчитайте объем 0,5% —ной соляной
кислоты, которую надо внести в воду, чтобы pH стал равным 6. Плотность раствора
кислоты принять равным 1 г/л.
Решение. Определяем концентрацию
ионов H+
в воде, которую надо приготовить. Используя формулу (7), получаем:
c(H+)
= 10‾ pH;
c(H+) = 10‾ 6
моль/л.
Т, к. при диссоциации одной
молекулы кислоты образуется один ион водорода (HCl = H+ + Cl‾),
можно считать, что концентрация кислоты, которую надо создать в растворе,
должна быть равна концентрации ионов водорода: c(HCl) = c(H+) = 10‾ 6 моль/л (концентрацией ионов водорода,
образующихся при диссоциации воды, можно пренебречь),
По формулам (4) и (5)
определяем массу HCl, которая должна содержаться в растворе:
m(HCl) = c(HCl) • V • M(HCl); m(HCl) = 10‾ 6
моль/л • 20 л • 36,5 г/моль=7,3 • l0‾ 4 г.
Рассчитываем массу 0,5% —
ного раствора кислоты, в котором содержится 7,3 • 10‾ 4 г HCl.
По формуле (2):
|
m = |
m(HCl) • 100 |
; |
m = |
7,3 • 10‾ 4
г • 100 |
= 0,146 г. |
|
w(HCl) |
0,5 |
Наконец, зная, что плотность раствора равна 1 г/мл, определяем, что в
аквариум надо внести 0,146 мл 0,5% —наго раствора HCl.
Следует отметить, приведенный расчет справедлив лишь для совершенно
чистой воды. Например, если в аквариум налить дистиллированную воду, то, внеся
рассчитанное количество кислоты, можно достичь требуемого значения pH. Если в
аквариуме используется водопроводная вода или вода из природных водоемов, в
которых растворены различные соединения, внесение рассчитанного количества
кислоты не приведет к желаемому сдвигу pH. В ряде случаев необходимое изменение
pH не достигается даже при внесении кислоты в десятикратном размере по
сравнению с рассчитанным количеством. Это происходит потому, что вода с
растворенными в ней веществами обладает буферными свойствами, т. е. является буферным
раствором.
Буферные растворы — это такие растворы, pH которых почти не зависит от разбавления
и почти не меняется при добавлении к ним небольших количеств кислот и щелочей.
Наиболее распространенные буферные растворы содержат, как правило, слабую
кислоту (CH3COOH, H2СO3, H3PO4 и др.) и соль этой же
кислоты. Например, буферными свойствами обладают смеси кислых и средних солей
одной кислоты или смеси двух кислых солей, например NaHCO3 + Na2CO3, NaH2PO4 + Na2HPO4. Смеси небольших равных
количеств NaH2PO4 и Na2HPO4 (или соответствующих
калиевых солей) позволяют поддерживать реакцию воды, близкую к нейтральной (pH
в интервале от 6,5 до 7,5).
Так называемый аммиачный буфер образует водный раствор аммиака и
какая-нибудь соль аммонии: NH4ОН + NH4Cl.
Буферные свойства аквариумной воды обусловлены содержанием в ней углекислоты H2СO3 и ее кислых солей Ca(HCO3)2
и Mg(HCO3)2.
Буферные растворы находят применение в тех случаях, когда надо
поддержать определенное значение pH. Они могут быть использованы аквариумистами
при лечении рыб, обеззараживании водной растительности, при борьбе с
вредителями аквариума, проведении химического анализа аквариумной воды и т. д.
О приготовлении буферных растворов можно прочитать в литературе по
аналитической химии (см. Лурье Ю. Ю. Справочник по аналитической химии. М.:
Химия, 1979).
Какова кислотность воды, в которой могут жить рыбы и водные растения?
Жизнь в воде возможна в довольно широком интервале pH: некоторые микроорганизмы
могут существовать в сильнокислой и сильнощелочной среде. В природных водоемах
значение pH колеблется в интервале от 3,2 до 10,5. Если говорить об аквариумных
рыбах, то интервал pH, пригодный для их содержания, несколько уже. В табл. 6
приведены значения pH некоторых природных водоемов в различных частях света. Во
всех перечисленных водоемах водятся рыбы, представляющие интерес для аквариумистов.
Таблица 6
Кислотность воды в некоторых природных водоемах.
|
Название водоема |
Место
расположения водоема |
Интервал
значений pH |
|
р. Маморе |
Ю.
Америка: Боливия |
6,0—8,0 |
|
р. Чучунак |
Ц.
Америка: Панама |
7,0—7,4 |
|
р. Ярдайн |
Австралия: п-ов Кейп-Йорк |
5,2—6,6 |
|
оз. Танганьика |
Африка: Танзания, Заир |
8,7—9,0 |
|
р. Ньонг |
Африка: Камерун |
5,7—6,2 |
|
р. Верде |
С.
Америка: Мексика |
6,9—7,3 |
|
р. Борай Пет |
Азия:
Таиланд |
5,8—6,8 |
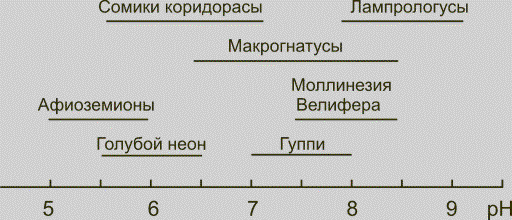
Рис.
4. Интервалы pH, в которых могут жить
некоторые аквариумные рыбы
Итак, для многих аквариумных
рыб подходит pH от 5 до 9. Однако для различных видов наиболее благоприятный
интервал кислотности еще уже. На рис. 4 показаны интервалы pH, в которых оптимально чувствуют
себя различные представители аквариумной ихтиофауны. Рыбы достаточно хорошо
адаптируются к изменению внешних условий, в том числе и к кислотности в
достаточно широких интервалах. Такая адаптация происходит наиболее полно при
выращивании в воде определенного состава нескольких поколений рыб. Поэтому
возможно содержание, а иногда и разведение рыб, при значениях pH, которые
выходят за рамки приведенных на рис. 4 интервалов, хотя наилучшие результаты
достигаются при определенном значении водородного показателя. На рис. 5
показана экспериментально установленная зависимость успешного спаривания
петушков (Betta splendens) от кислотности воды.
Наилучшие результаты были получены при значении pH близком к 7.
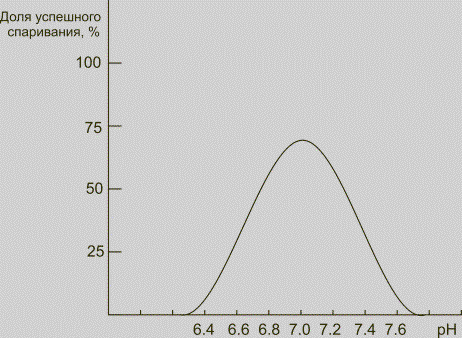
Рис. 5. Зависимость доли успешных спариваний
петушков от
pH
Если вы приобрели новых
аквариумных рыб, то желательно создать им условия, к которым они привыкли. Для
этого бывает необходимо изменить pH аквариумной воды. Если надо повысить
кислотность (уменьшить pH), можно воспользоваться кислотами. Лучше всего применять
уксусную и фосфорную кислоты. Можно использовать серную и соляную кислоты,
однако с большой осторожностью, т. к. при передозировке произойдет резкое
изменение pH. В качестве веществ, дающих кислую реакцию, используют
дигидрофосфаты калия, натрия или кальция: КH2PO4, NaH2PO4, Ca(H2PO4)2.
Иногда для подкисления воды применяют настой или отвар торфа, ольховых шишек,
которые содержат органические кислоты.
Щелочность можно поднять
(увеличить pH), используя растворы щелочей (NaOH, КОН), однако лучше воспользоваться
солями, имеющими щелочную реакцию: питьевой содой или гидрокарбонатом натрия NaHCO3, содой или карбонатом
натрия Na2CO3.
Может возникнуть вопрос,
почему некоторые соли (например, указанные здесь NaHCO3 и Na2CO3) используются для изменения
pH? Оказывается, водные растворы ряда солей имеют щелочную или кислую реакцию
вследствие гидролиза соли, т. е. взаимодействия ее с водой.
Например, соль NaHCO3 в воде диссоциирует на ионы:
NaHCO3 = Na+ + HCO3‾
Кислотный остаток слабой
угольной кислоты HCO3-взаимодействует с водой:
НСO3‾ + H2O= H2СO3 + ОН‾
в результате чего в воде
накапливаются гидроксидионы ОН‾, обеспечивающие щелочные свойства этой
соли.
Аналогичные процессы
протекают в растворе Na2CO3:
диссоциация: Na2CO3 = 2Na+ + СO32‾
гидролиз: СO32‾ + H2O = HCO3‾
+ ОН‾
причем во втором примере
гидролиз протекает в большей степени, чем в случае NaHCO3. Поэтому из растворов двух
солей (NaHCO3 и Na2CO3) последний будет обладать
более высоким значением pH.
Изменение кислотности воды
проводят очень осторожно: небольшое количество вещества надо растворить в воде
из аквариума (1—3 л) и полученный раствор добавлять при перемешивании
небольшими порциями. Для рыб безопасно изменение pH не более чем на 0,2 единицы
в течение часа.
Часто можно наблюдать такое явление, что
первоначально удается изменить кислотность аквариумной воды, однако довольно
быстро (иногда уже через сутки) pH принимает прежнее значение. Это говорит об
устойчивом равновесном состоянии аквариумной системы. Чтобы изменить кислотность
воды в таком аквариуме, придется провести в нем более значительные изменения:
заменить грунт, поменять воду, уменьшить число рыб. В аквариумах, так же как и
в природных водоемах, кислотность не остается постоянной: измеренные значения
pH могут оказаться различными в разное время суток, при изменении внешних
условий (а в природных водоемах — в различное время года). С чем связаны такие
колебания pH? Одна из важнейших причин, влияющих на кислотность аквариумной
воды — изменение содержания в воде углекислого газа, который хорошо
растворяется в ней с образованием угольной кислоты:
СO2 + H2O = H2СO3
Эта кислота диссоциирует с
образованием ионов водорода, обусловливающих кислую реакцию воды:
H2СO3
= H+ + HCO3‾
Можно назвать три основных
источника углекислого газа в аквариуме: растворение его из воздуха, с которым
контактирует вода (или которым продувается аквариум); выделение при дыхании рыб
и других животных; выделение углекислоты водными растениями в ночное время.
Изменение pH, связанное с CO2, может быть достаточно
сильным. Например, если в помещении в открытой банке оставить дистиллированную
воду, то ее pH обычно принимает значение 5,7— 5,8. Если воду специально
насытить углекислым газом, то можно достигнуть pH 4,8.
Если содержание углекислого
газа в воде уменьшается, то pH растет (т. е. кислотность уменьшается). Такие
процессы могут происходить под воздействием растений, которые на свету
поглощают CO2 из воды, Если грунт аквариума содержит карбонаты
(CaCO3, CaCO3), то они также реагируют с растворенным CO2. поглощая его из воды и
подщелачивая ее:
CO2 + CaCO3 + H2O
= Ca(HCO3)2.
Существует еще один фактор,
оказывающий существенное влияние на кислотность аквариумной воды. В аквариуме
всегда имеются бактерии Nitrosomonus, участвующие в разложении
азотосодержащих
H2O остатков, выделяемых рыбами. В процессе
жизнедеятельности бактерий выделяются ионы водорода H+, и происходит
подкисление воды. Особенно интенсивно этот процесс идет при использовании
аквариумных фильтров. Подкисление воды будет тем сильнее, чем больше рыб,
выделяющих соединения азота, содержится в аквариуме.
Процессы, влияющие на
кислотность аквариумной воды, представлены на рис. 6.
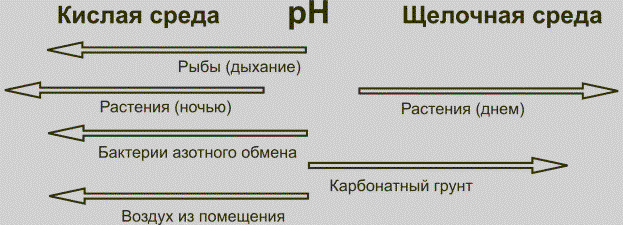
Рис.
6 Влияние различных факторов на
кислотность воды в аквариуме
Изменения кислотности воды в
аквариуме (особенно резкие) и смещение pH за пределы оптимальных интервалов
нежелательны, т. к. могут привести к заболеванию рыб. При этом рыбы «чешутся» о
грунт и растения, ведут себя беспокойно, при плавании совершают рывки, выпрыгивают
из воды. При появлении этих симптомов необходимо нормализовать значение pH в
аквариуме.
Чтобы не происходило резких
колебаний кислотности аквариумной воды, не следует перенаселять аквариум рыбами,
растениями и другими обитателями. Рекомендуется регулярно (еженедельно)
подменивать воду и постоянно контролировать pH.
Для измерения кислотности
воды в аквариуме используют индикаторы — вещества, которые изменяют окраску в зависимости от
pH. Например, индикатор метиловый оранжевый в растворе кислоты приобретет
красный цвет, а в растворе щелочи — желтый. Фенолфталеин в растворе щелочи
окрашивается в малиновый цвет, а в кислоте он бесцветен. Такие индикаторы
позволяют определить, является ли раствор кислым или щелочным.
Чтобы определить значение pH
раствора, можно использовать специальную индикаторную бумагу. Эта бумага
пропитана смесью различных индикаторов. Значение pH устанавливается путем
сравнения цвета бумаги, смоченной исследуемой водой, со стандартной цветной
шкалой. Точность определения pH при помощи такой бумаги невелика: обычно она
составляет 0,3— 0,5 единиц pH. При отсутствии навыка в использовании
индикаторной бумаги ошибка может быть велика,
Значительно точнее позволяет
измерить водородный показатель набор H. И. Алямовского, который также основан
на сравнении цветов. При этом цвет исследуемой воды с добавленным индикатором
сравнивается с окраской стандартных растворов, находящихся в запаянных ампулах.
Набор позволяет определить pH с точностью 0,1—0,2 единиц pH, что вполне
достаточно для любителя — аквариумиста. Разнообразные наборы для определения pH
предлагают иностранные и отечественные фирмы.
Наиболее точным методом
определения pH аквариумной воды является использование электронных приборов —
pH-метров. На рис. 7 показана принципиальная схема измерения. В стакан с
исследуемым раствором (1) погружают два электрода, входящие в комплект
pH-метра: стеклянный электрод (2) и хлорсеребряный электрод сравнения (3).
Электроды соединены с pH-метром (4): электрический сигнал с них поступает в
прибор. Между стеклянным электродом и электродом сравнения возникает разность
потенциалов E, которая связана со значением водородного
показателя. pH-метр построен по принципу вольтметра с высоким входным сопротивлением:
он измеряет значение разности потенциалов Е. Шкала прибора отградуирована в
единицах pH. Электронные pH-метры, если они хорошо настроены, позволяют
измерять водородный показатель с точностью 0,01 — 0,1 единицы pH, а иногда и
выше (в зависимости от марки прибора).

Рис.7.
Схема измерения pH при помощи pH-метра